Создание лекарственных средств
Весь процесс создания нового лекарственного соединения в ряде случаев может быть разделен на следующие этапы:
- поиск мишени (например, белка) действия нового лекарства;
- поиск низкомолекулярного соединения, обладающего нужным фармакологическим действием;
- изучение этого соединения в эксперименте;
- проведение испытаний в клинике.
Лишь малый процент возможных кандидатов на лекарство проходит успешное клиническое испытание. В среднем на разработку одного лекарства тратится от 1 до 2,5 млрд долларов и около 10–15 лет.
Суть лекарства — то есть то, что помогает человеку выздороветь — заключается в активном веществе. Вкупе с разнообразными химическими добавками оно может стать, например, удобной для проглатывания цветной таблеткой. Говоря о лекарствах далее, мы будем иметь в виду их активные вещества.
В организме человека протекает множество химических процессов. Их можно описать каскадами реакций (рис.1), которые могут быть очень большими и сложными. Развитие заболевания сопровождается нарушениями в каких-то химических процессах в организме. В каскадах реакций есть ключевые участники (некоторые молекулы, в большинстве случаев белки), которые в большей мере ответственны за происходящее. Для них, собственно, разрабатываются лекарства, то есть они становятся мишенями для них.
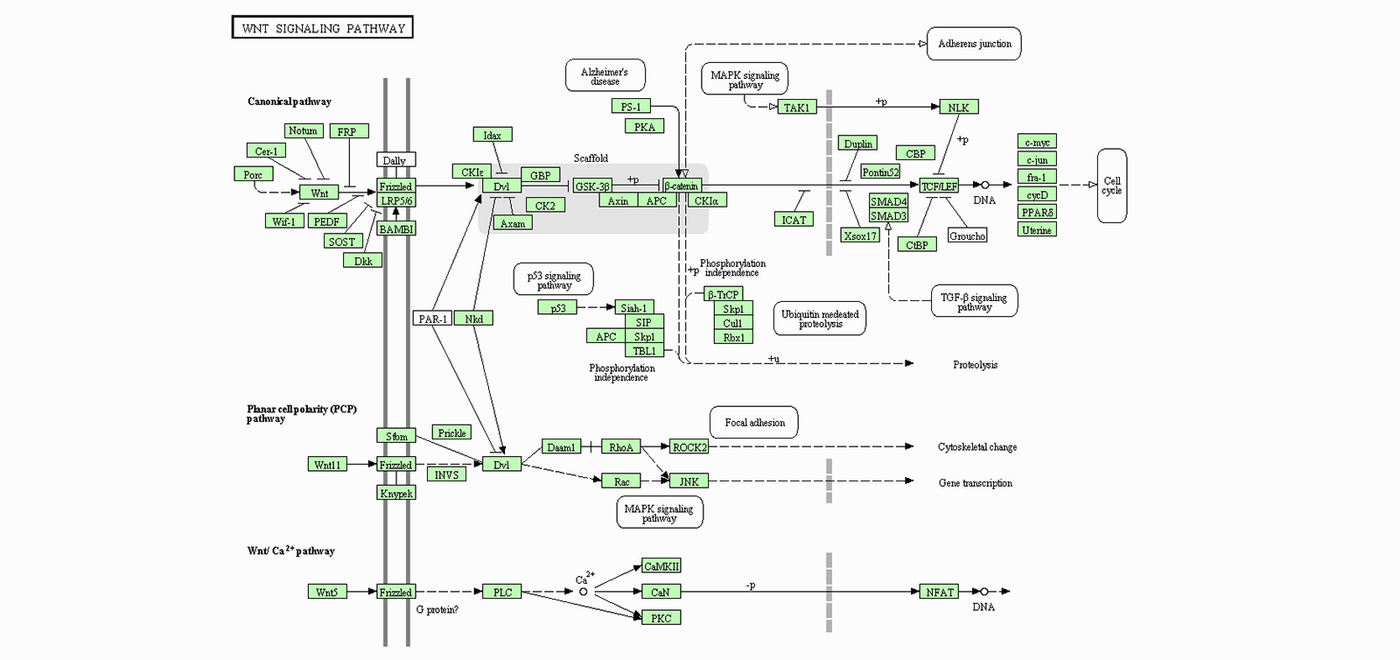
Рис.1 Пример сложного каскада реакций в нашем организме: сигнальный путь Wnt
Однако белки — большие молекулы. Поэтому мало просто вычислить белок как мишень среди каскадов и сетей, нужно еще и определить на этой мишени конкретное место. Его называют активным сайтом. Взаимодействие правильного лекарства с этим самым местом и должно приводить к желаемому результату — улучшению самочувствия или выздоровлению.
Представьте себе замок и ключ. Взаимодействие лекарства с белком-мишенью — это и есть закрывание или открывание замка ключом. Чтобы лекарственная молекула могла взаимодействовать с необходимым центром белка, она должна соответствовать множеству физических, химических и даже просто геометрических требований. Замок должен подходить к ключу. Итак, молекула, которая обладает лекарственной активностью против определенного заболевания, связывается с активным сайтом белка-мишени, что модулирует его активность (рис.2). Очень часто это модулирование заключается в ингибировании (подавлении) его взаимодействия с другими молекулами. Таким образом исправляются ошибки, то есть вылечивается заболевание. Однако важно заметить, что молекулярные механизмы воздействия лекарств на мишени и последующие изменения в каскадах реакций разнообразны и сложны.
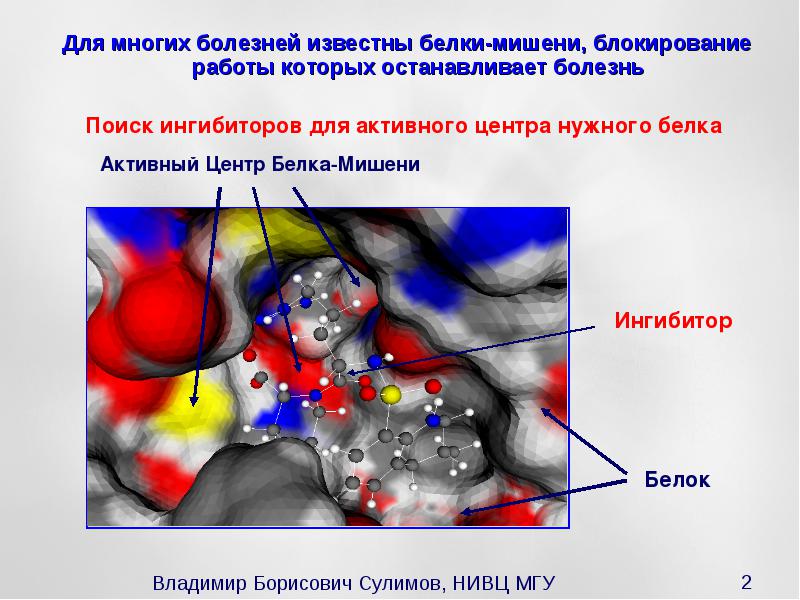
Рис.2 Поиск ингибиторов для активного центра нужного белка
Если пространственная структура белка-мишени известна, то вначале устанавливают место связывания низкомолекулярного соединения (лекарства) и белка-мишени. Затем проводят анализ полученного комплекса с помощью молекулярной графики (так называемый докинг) с последующим молекулярно-динамическим и квантовохимическим расчетом. Уже самый первый этап поиска подходящего кандидата на лекарство связан с перебором сотен миллионов вариантов из соответствующей базы данных низкомолекулярных соединений.
В случае, когда пространственная структура белка-мишени неизвестна, имеется достаточно большое число различных подходов сравнительного моделирования. При построении трехмерной модели белка с заданной аминокислотной последовательностью эта полипептидная цепочка сначала "вписывается" в координаты, соответствующие остаткам гомологичного белка с расшифрованной пространственной структурой, а затем осуществляется минимизация внутренней энергии, чтобы "убрать" возможные напряжения в структуре. В дальнейшем методами молекулярной динамики моделируется движение отдельных частей молекулы с целью уточнения расположения гибких участков. Качество полученной модели оценивают с использованием программы, которая сравнивает пространственное расположение аминокислотных остатков моделируемого белка с известной статистикой, полученной для белков с расшифрованной экспериментально пространственной структурой.
Построенные таким способом модели были успешно использованы для конструирования, например: новых ингибиторов протеазы вируса иммунодефицита человека для лечения СПИДа; ингибиторов ренина, как средства для лечения эссенциальной гипертензии; для белковой инженерии гибридных нейтрофорных факторов и т.д. Проект Elige.re имеет своей целью помощь в поиске новых лекарств, белков и других химических соединений.
Только зная все гены и белки организма, можно делать надежные выводы. Раньше для получения такого рода данных ставились специальные эксперименты, но представьте себе: у средней бактерии примерно 3000 генов, у человека – на порядок больше, 30 000, белков еще больше – сколько же надо провести экспериментов, например, для того, чтобы проверить все пары белков, взаимодействуют ли они. И при этом основное время как раз уйдет на "пустые" эксперименты, с невзаимодействующими белками. То же самое с функциями генов. В принципе, выяснение функции одного гена в эксперименте - это год работы сильного исследователя и хорошая статья. Но генов-то тысячи в каждом организме.
Все этапы таких исследований требуют высокопроизводительных вычислений.
Для решения таких ресурсоемких и сложных вычислительных задач применяются высокопроизводительные вычислительные системы, включающие суперкомпьютеры и компьютерные кластеры и распределенные вычисления.
Но об этом мы поговорим в следующей статье.
Олеся Унтевская,
специально для проекта Elige.re
По-английски: Creation of Medicinal Preparations